Приложение 3 к Инструкции о порядке назначения лекарственных средств и выписывании рецептов на них
Приложение 3 к Инструкции о порядке назначения лекарственных средств и выписывании рецептов на них
ПРЕДЕЛЬНО ДОПУСТИМОЕ КОЛИЧЕСТВО НАРКОТИЧЕСКИХ ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ ВЫПИСЫВАНИЯ В ОДНОМ РЕЦЕПТЕ
(введено Приказом Минздрава РФ от 09.01.2001 № 3)
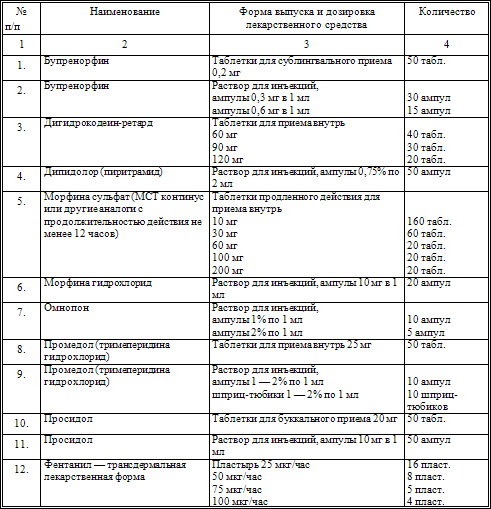
Примечания. 1. Нормы выписывания наркотических лекарственных средств для инкурабельных онкологических и гематологических больных могут быть увеличены в 2 раза против указанных в настоящем приложении.
2. При выписывании наркотических лекарственных средств, не вошедших в настоящую таблицу, их предельно допустимое количество для выписывания в одном рецепте может в пять раз превышать разовую дозу, указанную в утвержденной Фармакологическим комитетом Минздрава России инструкции по медицинскому применению выписываемого лекарственного средства.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
Статья 24. Реклама лекарственных средств, медицинской техники, изделий медицинского назначения и медицинских услуг, в том числе методов лечения
Статья 24. Реклама лекарственных средств, медицинской техники, изделий медицинского назначения и медицинских услуг, в том числе методов лечения 1. Реклама лекарственных средств не должна:1) обращаться к несовершеннолетним;2) содержать ссылки на конкретные случаи
Статья 24. Реклама лекарственных средств, медицинской техники, изделий медицинского назначения и медицинских услуг, в том числе методов лечения
Статья 24. Реклама лекарственных средств, медицинской техники, изделий медицинского назначения и медицинских услуг, в том числе методов лечения 1. Реклама лекарственных средств не должна:1) обращаться к несовершеннолетним;2) содержать ссылки на конкретные случаи
СТАТЬЯ 18. Ответственность за несоблюдение правил организации производства и контроля качества лекарственных средств и правил изготовления лекарственных средств
СТАТЬЯ 18. Ответственность за несоблюдение правил организации производства и контроля качества лекарственных средств и правил изготовления лекарственных средств 1. Организация – производитель лекарственных средств несет ответственность за несоблюдение правил
Глава VI. ВВОЗ ЛЕКАРСТВЕННЫХ СРЕДСТВ НА ТЕРРИТОРИЮ РОССИЙСКОЙ ФЕДЕРАЦИИ. ВЫВОЗ ЛЕКАРСТВЕННЫХ СРЕДСТВ С ТЕРРИТОРИИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Глава VI. ВВОЗ ЛЕКАРСТВЕННЫХ СРЕДСТВ НА ТЕРРИТОРИЮ РОССИЙСКОЙ ФЕДЕРАЦИИ. ВЫВОЗ ЛЕКАРСТВЕННЫХ СРЕДСТВ С ТЕРРИТОРИИ РОССИЙСКОЙ ФЕДЕРАЦИИ СТАТЬЯ 20. Порядок ввоза лекарственных средств на территорию Российской Федерации 1. Ввоз лекарственных средств, зарегистрированных в
СТАТЬЯ 41. Обязанность субъектов обращения лекарственных средств сообщать о случаях побочных действий и об особенностях взаимодействия лекарственных средств с другими лекарственными средствами
СТАТЬЯ 41. Обязанность субъектов обращения лекарственных средств сообщать о случаях побочных действий и об особенностях взаимодействия лекарственных средств с другими лекарственными средствами 1. Субъекты обращения лекарственных средств обязаны сообщать
«ОБ УТВЕРЖДЕНИИ ИНСТРУКЦИИ О ПОРЯДКЕ ИЗЪЯТИЯ ИЗ НЕЗАКОННОГО ОБОРОТА НАРКОТИЧЕСКИХ СРЕДСТВ, ПСИХОТРОПНЫХ ВЕЩЕСТВ И ИХ ПРЕКУРСОРОВ, ИНСТРУМЕНТОВ И ОБОРУДОВАНИЯ, НАХОДЯЩИХСЯ ПОД СПЕЦИАЛЬНЫМ КОНТРОЛЕМ И ИСПОЛЬЗУЕМЫХ ДЛЯ ПРОИЗВОДСТВА И ИЗГОТОВЛЕНИЯ НАРКОТИЧЕСКИХ СРЕДСТВ И ПСИХОТРОПНЫХ ВЕЩЕСТВ, А ТАКЖЕ ИХ
«ОБ УТВЕРЖДЕНИИ ИНСТРУКЦИИ О ПОРЯДКЕ ИЗЪЯТИЯ ИЗ НЕЗАКОННОГО ОБОРОТА НАРКОТИЧЕСКИХ СРЕДСТВ, ПСИХОТРОПНЫХ ВЕЩЕСТВ И ИХ ПРЕКУРСОРОВ, ИНСТРУМЕНТОВ И ОБОРУДОВАНИЯ, НАХОДЯЩИХСЯ ПОД СПЕЦИАЛЬНЫМ КОНТРОЛЕМ И ИСПОЛЬЗУЕМЫХ ДЛЯ ПРОИЗВОДСТВА И ИЗГОТОВЛЕНИЯ НАРКОТИЧЕСКИХ СРЕДСТВ
Приложение ИНСТРУКЦИЯ О ПОРЯДКЕ РЕГИСТРАЦИИ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ И МЕДИЦИНСКОЙ ТЕХНИКИ ОТЕЧЕСТВЕННОГО ПРОИЗВОДСТВА В РОССИЙСКОЙ ФЕДЕРАЦИИ
Приложение ИНСТРУКЦИЯ О ПОРЯДКЕ РЕГИСТРАЦИИ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ И МЕДИЦИНСКОЙ ТЕХНИКИ ОТЕЧЕСТВЕННОГО ПРОИЗВОДСТВА В РОССИЙСКОЙ ФЕДЕРАЦИИ к Приказу Минздрава Россииот 2 июля 1999 г. № 274ИНСТРУКЦИЯ О ПОРЯДКЕ РЕГИСТРАЦИИ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ И
«О РАЦИОНАЛЬНОМ НАЗНАЧЕНИИ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ПРАВИЛАХ ВЫПИСЫВАНИЯ РЕЦЕПТОВ НА НИХ И ПОРЯДКЕ ИХ ОТПУСКА АПТЕЧНЫМИ УЧРЕЖДЕНИЯМИ (ОРГАНИЗАЦИЯМИ)»
«О РАЦИОНАЛЬНОМ НАЗНАЧЕНИИ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ПРАВИЛАХ ВЫПИСЫВАНИЯ РЕЦЕПТОВ НА НИХ И ПОРЯДКЕ ИХ ОТПУСКА АПТЕЧНЫМИ УЧРЕЖДЕНИЯМИ (ОРГАНИЗАЦИЯМИ)» (ред. от 19.12.2003)(ИЗВЛЕЧЕНИЕ)В целях реализации Основ законодательства Российской Федерации об охране здоровья граждан
Приложение 1 ИНСТРУКЦИЯ О ПОРЯДКЕ НАЗНАЧЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ И ВЫПИСЫВАНИЯ РЕЦЕПТОВ НА НИХ (ИЗВЛЕЧЕНИЕ)
Приложение 1 ИНСТРУКЦИЯ О ПОРЯДКЕ НАЗНАЧЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ И ВЫПИСЫВАНИЯ РЕЦЕПТОВ НА НИХ (ИЗВЛЕЧЕНИЕ) УтвержденоПриказом Минздрава Россииот 23 августа 1999 г. № 328ИНСТРУКЦИЯ О ПОРЯДКЕ НАЗНАЧЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ И ВЫПИСЫВАНИЯ РЕЦЕПТОВ НА НИХ
Приложение 1 к Инструкции о порядке назначения лекарственных средств и выписывании рецептов на них
Приложение 1 к Инструкции о порядке назначения лекарственных средств и выписывании рецептов на них ПРЕДЕЛЬНО ДОПУСТИМОЕ КОЛИЧЕСТВО НЕКОТОРЫХ НАРКОТИЧЕСКИХ СРЕДСТВ, СИЛЬНОДЕЙСТВУЮЩИХ ВЕЩЕСТВ, ПРЕПАРАТОВ СПИСКА «А» И «Б», АНАБОЛИЧЕСКИХ ГОРМОНОВ, ПРОИЗВОДНЫХ
Приложение 4 ПОРЯДОК ОТПУСКА ЛЕКАРСТВЕННЫХ СРЕДСТВ В АПТЕЧНЫХ УЧРЕЖДЕНИЯХ/ОРГАНИЗАЦИЯХ
Приложение 4 ПОРЯДОК ОТПУСКА ЛЕКАРСТВЕННЫХ СРЕДСТВ В АПТЕЧНЫХ УЧРЕЖДЕНИЯХ/ОРГАНИЗАЦИЯХ УтвержденоПриказом Минздрава Россииот 23 августа 1999 г. № 328СогласованоМинистерство внутренних делРоссийской ФедерацииПОРЯДОК ОТПУСКА ЛЕКАРСТВЕННЫХ СРЕДСТВ В АПТЕЧНЫХ
Приложение к Правилам отпуска лекарственных средств из аптечных учреждений / организаций
Приложение к Правилам отпуска лекарственных средств из аптечных учреждений / организаций СИГНАТУРАНазвание органа управления размер 80 x 148 ммфармацевтическими организациями цветная полоскав субъекте Российской Федерации желтого цветашириной 1 смАптека №или
«О ПОРЯДКЕ ПРИНЯТИЯ РЕШЕНИЯ О ПРОВЕДЕНИИ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ ЛЕКАРСТВЕННЫХ СРЕДСТВ»
«О ПОРЯДКЕ ПРИНЯТИЯ РЕШЕНИЯ О ПРОВЕДЕНИИ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ ЛЕКАРСТВЕННЫХ СРЕДСТВ» (ИЗВЛЕЧЕНИЕ)В целях упорядочения организации клинических исследований лекарственных средств приказываю:1. Утвердить Инструкцию «О порядке принятия решения о проведении
«ОБ УТВЕРЖДЕНИИ ПОРЯДКА ВЫДАЧИ ЗАКЛЮЧЕНИЯ О СООТВЕТСТВИИ ОРГАНИЗАЦИИ ПРОИЗВОДСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ ТРЕБОВАНИЯМ ФЕДЕРАЛЬНОГО ЗАКОНА „О ЛЕКАРСТВЕННЫХ СРЕДСТВАХ“
«ОБ УТВЕРЖДЕНИИ ПОРЯДКА ВЫДАЧИ ЗАКЛЮЧЕНИЯ О СООТВЕТСТВИИ ОРГАНИЗАЦИИ ПРОИЗВОДСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ ТРЕБОВАНИЯМ ФЕДЕРАЛЬНОГО ЗАКОНА „О ЛЕКАРСТВЕННЫХ СРЕДСТВАХ“ В целях реализации положений Федерального закона от 22 июня 1998 г. № 86-ФЗ «О лекарственных средствах»
«ОБ УТВЕРЖДЕНИИ ПОЛОЖЕНИЯ О ПОРЯДКЕ ПРОВЕДЕНИЯ ГОСУДАРСТВЕННОГО КОНТРОЛЯ ЭФФЕКТИВНОСТИ И БЕЗОПАСНОСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ НА ТЕРРИТОРИИ РОССИЙСКОЙ ФЕДЕРАЦИИ»
«ОБ УТВЕРЖДЕНИИ ПОЛОЖЕНИЯ О ПОРЯДКЕ ПРОВЕДЕНИЯ ГОСУДАРСТВЕННОГО КОНТРОЛЯ ЭФФЕКТИВНОСТИ И БЕЗОПАСНОСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ НА ТЕРРИТОРИИ РОССИЙСКОЙ ФЕДЕРАЦИИ» В соответствии с Федеральным законом от 22.06.1998 № 86-ФЗ «О лекарственных средствах» (с изменениями и
Статья 24. Реклама лекарственных средств, медицинской техники, изделий медицинского назначения и медицинских услуг, в том числе методов лечения
Статья 24. Реклама лекарственных средств, медицинской техники, изделий медицинского назначения и медицинских услуг, в том числе методов лечения 1. Реклама лекарственных средств не должна:1) обращаться к несовершеннолетним;2) содержать ссылки на конкретные случаи